合成生物学诞生于21世纪初,是生物学、工程学、化学和信息技术等相互交叉融合的新兴领域,利用基因组测序、生物工程、化学合成和计算机模拟等技术进行生命设计与合成再造,突破原有生物系统的限制,创造出更加符合产业化的新型生物系统。
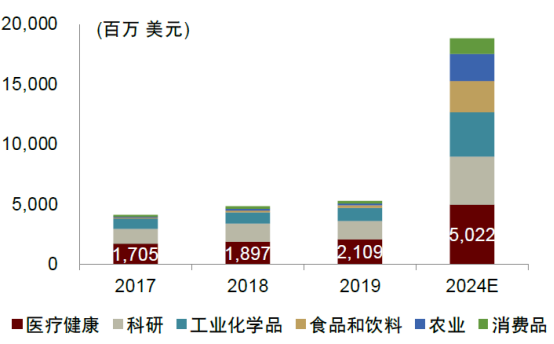
合成生物技术发展将对现有传统技术起到良性的补充作用,并在未来对传统技术进行合理化的替代,最终稳步覆盖医疗、化工、食品、农业、消费品等终端领域。据CB Insights预计,全球合成生物学市场规模从2019年的53亿美元增长到2024年的189亿美元(CAGR 28.8%)。其中,合成生物学在医疗健康领域的市场规模从2019年的21亿美元增长到2024年的50亿美元(CAGR 18.9% ),2019年其占比达到40%,是第一大应用领域。
RNA药物分为寡核苷酸药物和mRNA 药物。其中,寡核苷酸药物又可细分为RNA 干扰(RNAi)、RNA激活(RNAa)和核酸适配体(Aptamer)等类型。美国公司Ionis 和Alnylam是寡核苷酸方向比较有代表性的公司,德国公司BioNtech和美国公司Moderna则是mRNA疗法方向比较有代表性的公司。在新型冠状病毒肺炎(COVID-19)流行期间,mRNA技术在快速开发疫苗方面的优势凸显,Moderna公司开发的mRNA-1273在25天内完成了COVID-19疫苗的序列设计和生产,并破纪录地用63天完成从序列设计到首个受试者给药。目前,该疫苗已于2020年底获得FDA紧急使用授权。
中国的RNA疗法也开始发展,大批归国人才携技术和资源创业,多在江浙一带落户,形成独特的小核酸产业集群。十多年来,在政策逐渐放开,资本逐渐聚拢的良性环境下,国内RNA企业稳步发展。像艾博生物,斯微生物和深信生物都是国内比较出色的RNA公司。
艾博生物专注于mRNA 疫苗研发、分子设计、递送系统等技术领域。2020年6月,艾博生物联合军事科学院军事医学研究院、云南沃森生物共同研制的新型冠状病毒mRNA疫苗(ARCoV),正式通过国家药品监督管理局药物临床试验审批,进入临床I 期研究阶段,成为中国首个进入临床阶段的mRNA 疫苗。9月ARCoV也获印度尼西亚食品药品监督管理局(BPOM)颁发紧急用途许可证(EUA)。
斯微生物,涵盖了药物研发、递送系统设计、mRNA合成和生产,前后向一体化程度颇深。技术层面上,斯微生物采用了LPP纳米递送平台,即双层外壳的磷脂结构,相比传统的单层结构,LPP具有更好的包载、保护mRNA 的效果,并能够随聚合物的降解逐步释放mRNA 分子。
深信生物主要在感染性疾病预防疫苗、罕见病、肿瘤治疗性疫苗、肿瘤免疫治疗增强剂四大方向构建研发管线,目前该公司多个管线同步进行中。在技术层面上,深信生物在研发方法、递送路径等方面与国际mRNA研发三巨头(Moderna/BioNtech/Curevac)保持同步,其独有知识产权的LNP 递送平台,可以满足不同类型的mRNA 药物对递送的需求,是国际上少数拥有mRNA递送技术核心的公司,处于国际领先水平。
目前商用的基因编辑技术主要包括锌指核酸酶、转录激活因子样效应核酸酶和CRISPR3种类型。
Emmanuelle Charpentier 等人创办的瑞士公司CRISPR 主要研究CRISPR/Cas9 基因编辑技术及其在β 地中海贫血、血友病、杜氏肌营养不良症、囊性纤维化等疾病治疗中的应用。
美国公司Sangamo专注于锌指蛋白技术的研究和商业化开发,是全球应用锌指蛋白技术的代表性公司,在血友病、血红蛋白病、中枢神经系统疾病和艾滋病等疾病方面均有管线布局。
张锋等人创办的美国公司Editas Medicine 正在开发基于CRISPR/Cas9技术的基因组编辑平台,该公司在眼睛疾病、肌肉疾病、血液疾病、肺病、肝病和癌症等方面均有管线布局。
2015 年创立的异种器官移植公司eGenesis利用CRISPR 技术将猪开发为可行的人类器官移植来源。目前,eGenesis正在将改造的基因工程猪的器官移植到非人灵长类动物(如猴子)身上,进行长达一年的跟踪观察,并计划于2022 年底申请新药临床试验(IND)许可。eGenesis的姊妹公司启函生物于2017 年在杭州创立,并于2021 年 3月完成了 6 700 万美元的 A++轮融资,用以推进新型细胞治疗的研发。基于其科研团队在异种器官移植动物模型中积累的丰富经验,启函生物在未来将致力于寻找人体细胞中影响免疫排斥反应的基因,并通过编辑这些基因来提高细胞的免疫兼容性,实现低风险的同种异体细胞治疗。目前,启函生物正在应用这一方法,基于临床级GMP 干细胞,研发用于临床试验的细胞治疗产品。
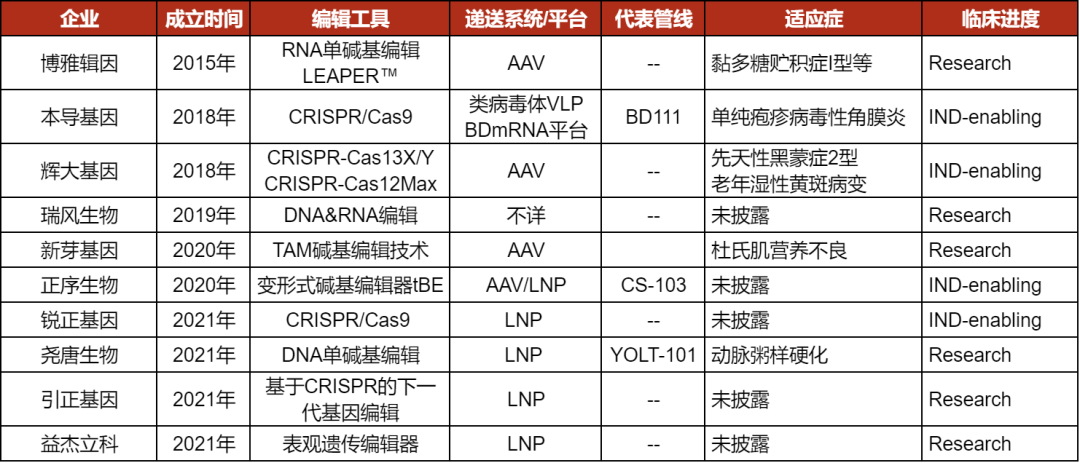
近年来,我国科学家在基因编辑领域取得了令人鼓舞的进展,在基因编辑系统发展、机制研究、构建基因编辑动植物模型和基因治疗等方面取得了突出的成绩。也涌现出一批致力于先进基因编辑疗法开发的企业,其中包括邦耀生物、博雅辑因、瑞风生物、引正基因、本导基因、辉大基因、新芽基因、锐正基因、正序生物、尧唐生物、科金生物、益杰立科等几十家公司。
细胞免疫疗法是抽取外周血中的免疫细胞种子,通过一定的技术手段筛选、激活并扩增我们想要的免疫细胞,再输回体内进行“战斗”。
它的优势包括:(1)能为患者提供长期持续的疾病管理(2)可利用内源性细胞产生协调反应(3)可利用合成生物学对其功能进行精准控制。经过改良的细胞系统已证明了其对提高检测和攻击癌细胞、通过药物或抗原控制治疗、分化干细胞以形成复杂组织的能力。
利用逻辑计算提高特异性。嵌合抗原受体(CAR)T细胞疗法已经获临床批准,可以应用在几种血癌中,甚至对放疗和化疗失败的患者也有效。更精准的治疗可以通过感应和响应抗原组合设计具有更大特异性的细胞疗法。遗传逻辑线路(与门、或门和非门)是合成生物学中基本的细胞决策系统,可以整合多个输入信号。为了减少患者因肿瘤抗原逃逸而复发,双特异性OR-gate CARs在工程免疫细胞的细胞外表面显示两个独特的单链抗体片段,并可被多种抗原激活。OR-gate CARs的缺点包括潜在的致命CRS、神经毒性和B细胞再生障碍性疾病等。神经毒性是目前CAR疗法的危险副作用,会导致22%的患者出现精神错乱、谵妄、语言障碍和癫痫发作。
利用生死开关和活动开关加强控制。利用合成生物学策略可以提高细胞治疗的安全性,包括药物诱导的安全开关。其中比较成功的是一种药物诱导型半胱天冬酶9(iCasp9)生死开关(kill switches),由Bellicum制药公司授权,用于CAR-T细胞和组织相容性白细胞抗原(HLA)不匹配造血干细胞移植(HSCTs)的20多个临床试验。生死开关的主要限制是其最终结果:一旦激活,治疗细胞就会从患者体内移除。为此,开发了基于非半胱天冬酶效应器的FKBP12/AP1903二聚系统的活动开关。
现有细胞疗法的通用平台。另一种控制受体介导的细胞治疗策略是将受体分成两个独立部分:由细胞内信号成分和细胞外对接结构域组成的通用CAR,以及用于选择不同目标和滴定以产生特定激活程度的模块化对接适配器。Cogent Bio公司设计的首个进入临床试验的分离CAR,其显著优点是能够使用任何抗体来控制抗原靶向,并且CAR - T细胞可以根据需要通过不同的抗体重新定向。
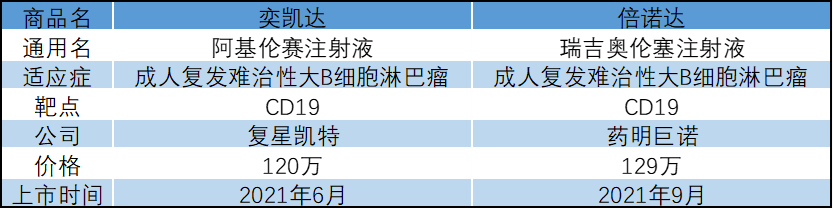
FDA批准的6款CAR-T疗法

中国上市的两款CAR-T疗法
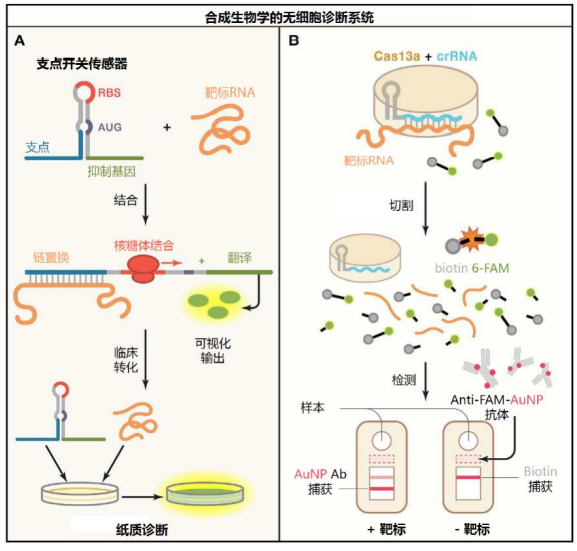
基于基因线路构建和快速迭代原型的合成生物学技术也在逐步推动了诊断方法的改进和创新,大大提高了定量的灵敏度、特异性和准确性,及改进分析特性(减少诊断时间、降低成本、提高可移植性、简化工作流程等)。如工程化的RNA支点开关适用于特定核酸的生物医学诊断,可以与无细胞表达系统结合,创建高度便携的纸质核酸诊断。基于CRISPR 的技术的“附带切割”的Cas效应器可以作为高度敏感且易于编程的核酸探测器。其中两种——SHERLOCK反应和DETECTR 反应,已被美国FDA授予紧急使用许可,用于检测人类临床样本中的新冠病毒。
基于合成生物学技术的细菌工程化改造为肿瘤治疗提供了全新的思路,细菌疗法因其具有良好的靶向性、较低的毒副作用,日益得到重视。早在200多年前,医生们就注意到了细菌感染有时会减缓肿瘤生长甚至将其根除。William Coley 医生将细菌灭活,制成了“科利毒素”(Coley’s toxins),最终成功治疗了超过1 000 名肿瘤患者,这种治疗方法的成功率居然与现代的癌症治疗方法不相上下。
利用合成生物学技术生产微生物药物的代表——美国上市公司Synlogic通过合成生物学技术改造益生菌,从而开发新型的活性药物SyntheticBioticTM。Synlogic主要关注机能失调以及其他因素引起的疾病,同时也与罗氏、Ginkgo Bioworks等公司合作,开发罕见疾病、代谢疾病、自身免疫和炎性疾病以及癌症等疾病的合成生物药物。
在噬菌体疗法方向,以色列公司BiomX正使用天然及合成的噬菌体治疗慢性疾病(如炎症性肠病)和皮肤病,该公司于2019 年成功上市,是全球首家噬菌体疗法上市公司。
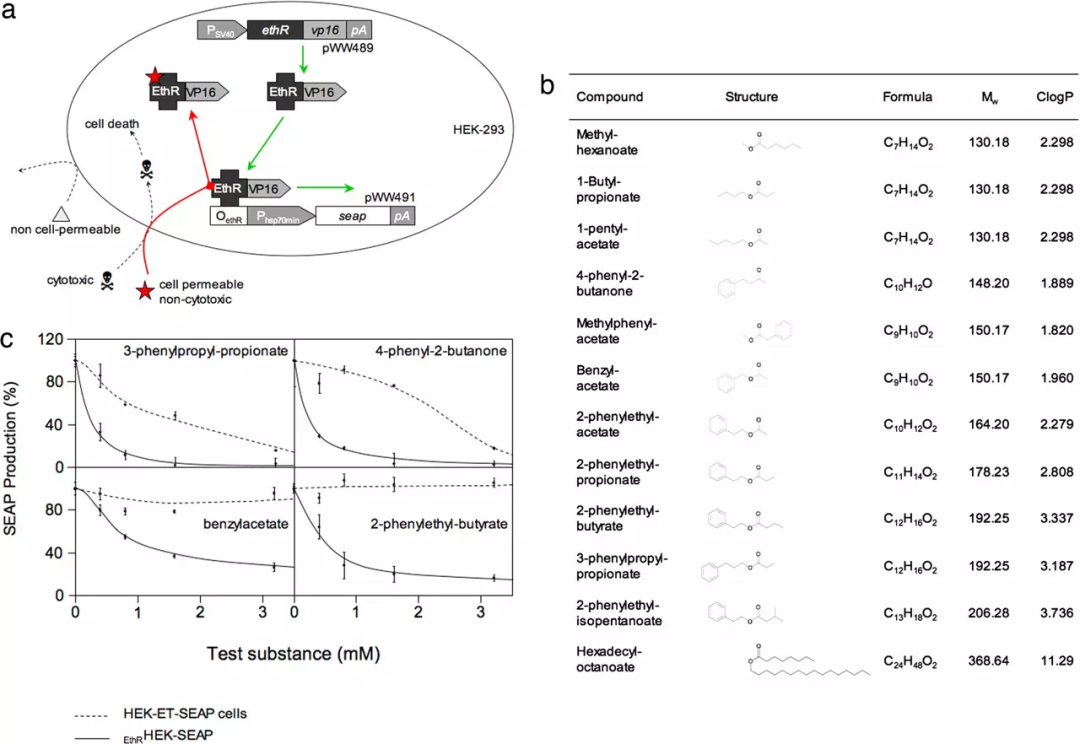
用于药物筛选的合成哺乳动物基因回路(来源:PNAS [16])
除此之外,合成生物学也为发现新型抗癌药物提供了全新的方法论。细胞毒性抗癌药物被认为通过靶向DNA复制并优先杀死活跃分裂的细胞来区分癌组织和正常组织,一项研究便通过设计改造细胞系,使其模仿肿瘤细胞的特征以用作新型抗癌药物的高通量筛选。 最后,药物生产也是细胞层面上合成生物学的关键应用,合成生物领域的代表性案例 “抗疟疾药物青蒿素前体的生物合成” 长期以来便为人所津津乐道。当然,可以通过生物合成的自然不仅仅是小分子药物,比如单克隆抗体,也是可以通过重组的方式来进行生产。






